摘要:
在临床实践中,糖尿病、脂肪肝、高脂血症等常常伴发出现。一般来说,肥胖症患者常伴发 2 型糖尿病,但临床上,体重未达到病态肥胖的 2 型糖尿病患者也不在少数。常用的代谢外科治疗手段,例如胃旁路手术(RYGB),其作为减重代谢外科的主流术式,主要作用之一便是减重,十二指肠空肠套管术(DJBS)作为模拟 RYGB 手术原理的内镜介入疗法,其主要疗效也是减重。因此,部分学者推断:RYGB 或 DJBS 的降糖疗效是通过减重而来的,减得越多,血糖降得越快。那么,较低 BMI(非病态肥胖)的患者是否同样适用 DJBS 术?其降糖疗效是否又能与病态肥胖患者保持一致呢?
正文:
DJBS 是一种通过胃镜介入放置在十二指肠空肠内的膜管样装置,其可以阻止营养物质与近端肠道之间的接触,从而减少吸收,达到治疗效果。在对患有 2 型糖尿病(T2DM)的病态肥胖患者(平均 BMI 为 38.9~44.8 kg/m2)的研究中[1,2],空腹血浆葡萄糖(FPG)在置入 DJBS 后 1 周内出现下降,并维持到 52 周和 24 周,这表明 DJBS 可能是 T2DM 的一种有效治疗方法。
但其实大多数糖尿病患者的 BMI 并不处于病态肥胖范围,而是在 30 kg/m2 左右的轻中度肥胖范围[3]。那么,对于这种较低 BMI 的糖尿病患者,DJBS 能否也起到控制糖尿病的效果呢?
目前的指南指出,减肥手术应限于 BMI≥35 kg/m2 的患者[4],但仍有一些研究报告了 BMI<35 kg/m2 的 T2DM 患者的结果。笔者对最近发表的 29 项关于 BMI<35 kg/m2 的 T2DM 患者代谢手术的研究进行了回顾,结论是这些手术也可以使患者 BMI、FPG 和 血红蛋白 A1c(HbA1c)达成在统计学上的显著下降[5]。
一项来自于巴西的“十二指肠空肠套管术在较低 BMI 糖尿病患者的适用性研究”同样解答了这个问题[6]。这是一项为期 52 周的前瞻性、开放标签、单中心的临床研究,研究招募了一批年龄在 18 至 55 岁之间的成年男性和女性,患 T2DM 的时间为 10 年左右,正在接受口服降糖药物治疗。其他入选标准包括 HbA1c 为 7.5%-10%,BMI 为 26-50 kg/m2(然而因为研究者对低 BMI 受试者的 T2DM 感兴趣,所以最终有效的 BMI 上限为 36kg/m2)。
最终有 20 名患者成功进行了 DJBS 术,这 20 人平均年龄为 49.8±6.7 岁,平均 BMI 为 30.0±3.6 kg/m2,T2DM 的平均持续时间为 6.6 ± 3.1 年。在 20 名被置入的受试者中,有 16 人(80%)完成了 12 个月的 DJBS 治疗。置入时间的算数平均数和中位数是 348 天和 365 天。在置入期间,患者体重、BMI、FPG、HbA1c都有明显的下降。低密度脂蛋白和甘油三酯在第 4 周时显示出大幅下降,并在研究结束时一直保持较低水平。高密度脂蛋白胆固醇水平没有明显变化。(表1)
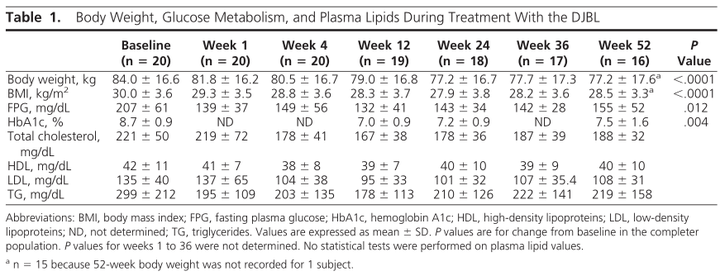
表1 高密度脂蛋白胆固醇水平变化
基于本研究的结果,DJBS 在迅速降低 FPG 的能力方面与代谢手术相似,这代表了 DJBS 作为一种非手术方法,可能可以阻止或逆转 BMI<35 kg/m2 患者的血糖状况和血脂水平。也就是说,并非体重越重,减重越多,降糖效果就越好。轻度、中度肥胖的 T2DM 患者也能通过 DJBS 达到良好的降糖和控制心血管风险的疗效。此外,本研究通过英国前瞻性糖尿病研究风险引擎[7]来估计其他风险状况的变化时,发现在完成 1 年治疗的 16 名受试者中,其冠心病的平均 10 年风险从 13.4% 下降到 12.2%。

图 1 胃转流支架系统置入后身体各项指标变化
类似的结论在国内也得到了验证,一项来自中国杭州的研究显示[8],采用国产 DJBS 设备“胃转流支架系统”(TONGEE®DJBS)的临床研究中,招募患者的平均 BMI 在 32.6 ± 3.9 kg/m2,置入支架三个月后,HbA1c 水平显著降低(6.3±1.7% vs. 5.6±0.6%,P < 0.05),并且这一差异在支架移植后 6 个月仍有统计学意义。此外,研究发现支架的置入迅速降低了胰岛素抵抗指数(HOMA-IR),HOMA-IR 在置入后 3 个月显著降低(6.0 ± 5.4 vs 3.7 ± 2.9,P < 0.05)。这些结果为“胃转流支架系统”在非病态肥胖 T2DM 患者中的应用提供了理论基础,未来或将为非病态肥胖 T2DM 患者带来显著的临床获益。(图 1)
综上所述,多数研究提示,DJBS 和“胃转流支架系统”这类内镜介入的非手术疗法能够改善非病态肥胖 T2DM 患者的血糖状况。由于目前已发表的研究随访时间相对较短,手术的长期获益尚不明确,仍需进一步研究探索。这些研究若能证实,将对内镜介入干预 T2DM 治疗的临床工作作出重要的指导意义,甚至可能改变目前临床上主要依靠药物治疗 T2DM 的现状。
参考文献:
[1]Rodriguez L, Reyes E, Fagalde P, et al. Pilot clinical study of an endoscopic, removable duodenal-jejunal bypass liner for the treatment of type 2 diabetes. Diabetes Technol Ther. 2009;11(11):725-732. doi:10.1089/dia.2009.0063
[2]de Moura EG, Martins BC, Lopes GS, et al. Metabolic improvements in obese type 2 diabetes subjects implanted for 1 year with an endoscopically deployed duodenal-jejunal bypass liner. Diabetes Technol Ther. 2012;14(2):183-189. doi:10.1089/dia.2011.0152
[3Nguyen NT, Nguyen XM, Lane J, Wang P. Relationship between obesity and diabetes in a US adult population: findings from the National Health and Nutrition Examination Survey, 1999-2006. Obes Surg. 2011;21(3):351-355. doi:10.1007/s11695-010-0335-4]
[4] Bariatric surgery: An IDF statement for obese Type 2 diabetes. Obes Res Clin Pract. 2011;5(3):e169-e266. doi:10.1016/j.orcp.2011.07.002
[5] Reis CE, Alvarez-Leite JI, Bressan J, Alfenas RC. Role of bariatric-metabolic surgery in the treatment of obese type 2 diabetes with body mass index<35 kg/m2: a literature review. Diabetes Technol Ther. 2012;14(4):365-372. doi:10.1089/dia.2011.0127
[6] Cohen RV, Neto MG, Correa JL, et al. A pilot study of the duodenal-jejunal bypass liner in low body mass index type 2 diabetes. J Clin Endocrinol Metab. 2013;98(2):E279-E282. doi:10.1210/jc.2012-2814
[7] Stevens RJ, Kothari V, Adler AI, Stratton IM; United Kingdom Prospective Diabetes Study (UKPDS) Group. The UKPDS risk engine: a model for the risk of coronary heart disease in Type II diabetes (UKPDS 56) [published correction appears in Clin Sci (Lond) 2002 Jun;102(6):679]. Clin Sci (Lond). 2001;101(6):671-679.
[8] Ren M, Zhou X, Yu M, et al. Prospective study of a new endoscopic duodenal-jejunal bypass sleeve in obese patients with nonalcoholic fatty liver disease (with video) [published online ahead of print, 2022 Jul 23]. Dig Endosc. 2022;10.1111/den.14409. doi:10.1111/den.14409